
https://www.happycampus.com/report-doc/24937017/
[일반화학실험 A+리포트] 분광법을 이용한 금속이온의 정량분석 레포트
Ⅰ. Title: 분광법을 이용한 금속이온의 정량분석(Spectrophotometric analysis of metal ions) Ⅱ. Objectives 1. 표준용액 제조에 필요한 몰 농도를 계산할 수 있다. 2. Stock solution을 희석하여 다양한 농도의 표준
www.happycampus.com
(위 링크확인)
* 전체 내용은 해피캠퍼스에 제가 등록해놓은 자료를 통해 확인하실 수 있습니다.
Ⅰ. Title: 분광법을 이용한 금속이온의 정량분석(Spectrophotometric analysis of metal ions)
Ⅱ. Objectives
1. 표준용액 제조에 필요한 몰 농도를 계산할 수 있다.
2. Stock solution을 희석하여 다양한 농도의 표준용액을 만들 수 있다.
3. 표준용액으로부터 얻은 흡광도 데이터를 이용하여 Beer 법칙 그래프를 그릴 수 있다.
4. Beer 법칙 그래프로부터 금속이온의 미지 농도를 알아낼 수 있다.
Ⅲ. Background Information
1. 전자기파 [1]

자외선(ultraviolet), 가시광선(visible)과 같은 복사선이 투명한 물질 층을 통과하는 경우 특정 주파수(=에너지)의 복사선세기가 선택적으로 감소되는 경우가 있는데, 이러한 현상을 흡수(absorption)이라고한다. 이때 빛 에너지의 일부는 물질의 원자 또는 분자로 이동되고, 특히 자외선과 가시광선에 해당하는 에너지의 빛은 분자의 최외각 전자(valance electron)를 높은 에너지상태로 여기(excitation)시킨다. 그 결과 분자는 바닥 에너지 상태(ground state)에서 들뜬 상태(excited state)로 된다. 약 400~750 nm 파장대의 빛은 가시광선 영역이다. 이에 해당하는 에너지의 빛은 사람의 눈에 색깔로 나타나 보이게 된다.
전이금속(transition metal) 이온과 리간드(ligand)가 배위결합(coordination bonding)을 하여 형성하는 배위화합물(또는 착화합물, coordination complex)은 분자내의 최외각 전자가 들뜬 상태로 여기되는 데 필요한 에너지가 가시광선 파장대에 해당하는 경우가 많고, 따라서 전위금속 배위화합물은 색을 띄는 경우가 많다. 단 사람이 특정물질의 색을 볼 때, 물질이 내는 빛을 관찰하는 것이 아니라 반사된 빛을 보는 것이다. 같은 맥락으로 우리의 눈이 감지하는 색은 분자가 흡수하는 빛의 파장의 색이 아니라 그것의 보색(complementary color)이다.
| Absorbed color | Absorbed wavelengths [nm] | Complementary color |
| Violet | 380-435 | Yellow-green |
| Blue | 435-480 | Yellow |
| Green-blue | 480-490 | Orange |
| Green | 490-560 | Red |
| Yellow-green | 560-595 | Purple |
| Orange | 595-650 | Green-blue |
| red | 650-780 | Blue-green |
[table 1] 화합물에 흡수된 빛의 색과 관찰되는 색 사이의 관계
2. 전자기파의 상호작용[2]
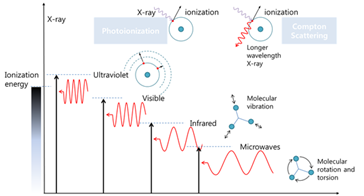
전자기파는 그 종류별로 원자와 다양한 종류의 상호작용을 한다.
a) 라디오파, 감마선 <-> 원자핵
b) X-ray <-> 중심전자
c) UV <-> 최외각 전자의 전자전이
d) IR <-> 최외각전자의 진동전이
e) 마이크로파 <-> 최외각전자의 회전전이
3. Beer-Lambert’s Law [3]
분광광도계(spectrophotometer)를 이용한 흡수분광법(absorption spectroscopy)를 사용하면, 용액중의 특정분자가 빛을 흡수하는 성질을 이용하여 시료의 농도를 측정할 수 있다. 농도가 높을수록 흡수되는 빛의 양은 많아지고, 농도가 낮을수록 흡수되는 빛의 양은 적어지므로 용액을 투과한 빛의 세기를 측정하고 비교, 분석하는 조작을 통하여 정량분석(quantative analysis)을 할 수 있다. 분광광도계는 일반적으로 광원, 서로 다른 파장으로 빛을 분리하는 회절격자, 샘플홀더 및 샘플을 통과하는 빛의 양을 감지하는 감지기(detector)를 포함한다.
농도와 흡광도(absorbance)의 비례적 관계를 가장 잘 설명하는 것이 Beer-Lambert 법칙이다. 이에 따르면 광원으로부터 조사된 빛이 <후략> 위 링크에서 전체내용을 확인하세요
Ⅳ. Materials
: UV-Vis 분광광도계, 큐벳(cuvette), 50mL 비커, 100mL 비커, 50mL 부피 플라스크, 10mL 부피 플라스크, 1mL 피펫, 5mL 피펫, 킴와이프스(kimwipes, 세척 티슈), 0.2M CuSO4∙5H2O , 증류수
Ⅴ. Procedures
<실험 과정은 위 링크에서 확인할 수 있습니다>
실험 A. Stock solution(0.2M CuSO4∙5H2O 용액) 50mL 제조
실험 B. Stock solution(0.2M 용액) 50mL 제조
실험 C. 흡광도 측정
Ⅵ. Results and Discussion
<상단 링크에서 전체 내용 확인하기>
Ⅷ. Reference
[1] 한국방송통신전파진흥원,
available from: https://emf.kca.kr/html/elecBusiness/class.do?menuCd=FM0802
[2] 조지아 주립대, Hyper Physics,
available from: http://hyperphysics.phy-astr.gsu.edu/hbase/mod3.html
[3] GIST, 일반화학실험, 2019, 18_분광법을 이용한 금속이온의 정량분석
[3] WILLY, available from:https://sites.google.com/a/maricopa.edu/willy/home/chemistry/12712
https://www.happycampus.com/report-doc/24937017/
[일반화학실험 A+리포트] 분광법을 이용한 금속이온의 정량분석 레포트
Ⅰ. Title: 분광법을 이용한 금속이온의 정량분석(Spectrophotometric analysis of metal ions) Ⅱ. Objectives 1. 표준용액 제조에 필요한 몰 농도를 계산할 수 있다. 2. Stock solution을 희석하여 다양한 농도의 표준
www.happycampus.com
(위 링크확인)
* 전체 내용은 해피캠퍼스에 제가 등록해놓은 자료를 통해 확인하실 수 있습니다.
'해피캠퍼스' 카테고리의 다른 글
| [일반화학실험 A+리포트] 얇은 막 크로마토그래피 (TLC) (0) | 2021.11.06 |
|---|---|
| [일반화학실험 A+리포트] 재결정과 녹는점 측정 (0) | 2021.11.06 |
| [일반화학실험 A+리포트] 아스피린 합성과 분석 (0) | 2021.11.06 |
| [일반화학실험 A+리포트] 분자모델링 VSEPR (0) | 2021.11.06 |
| [일반화학실험 A+리포트] 정확도와 정밀도(Accuracy and precision) (0) | 2021.11.06 |
![[일반화학실험 A+리포트] 분광법을 이용한 금속이온의 정량분석](https://img1.daumcdn.net/thumb/R750x0/?scode=mtistory2&fname=https%3A%2F%2Fblog.kakaocdn.net%2Fdn%2Fb0MI8v%2FbtrkembxbdF%2FwNjHRjv16E6zPbf5VToPE0%2Fimg.png)